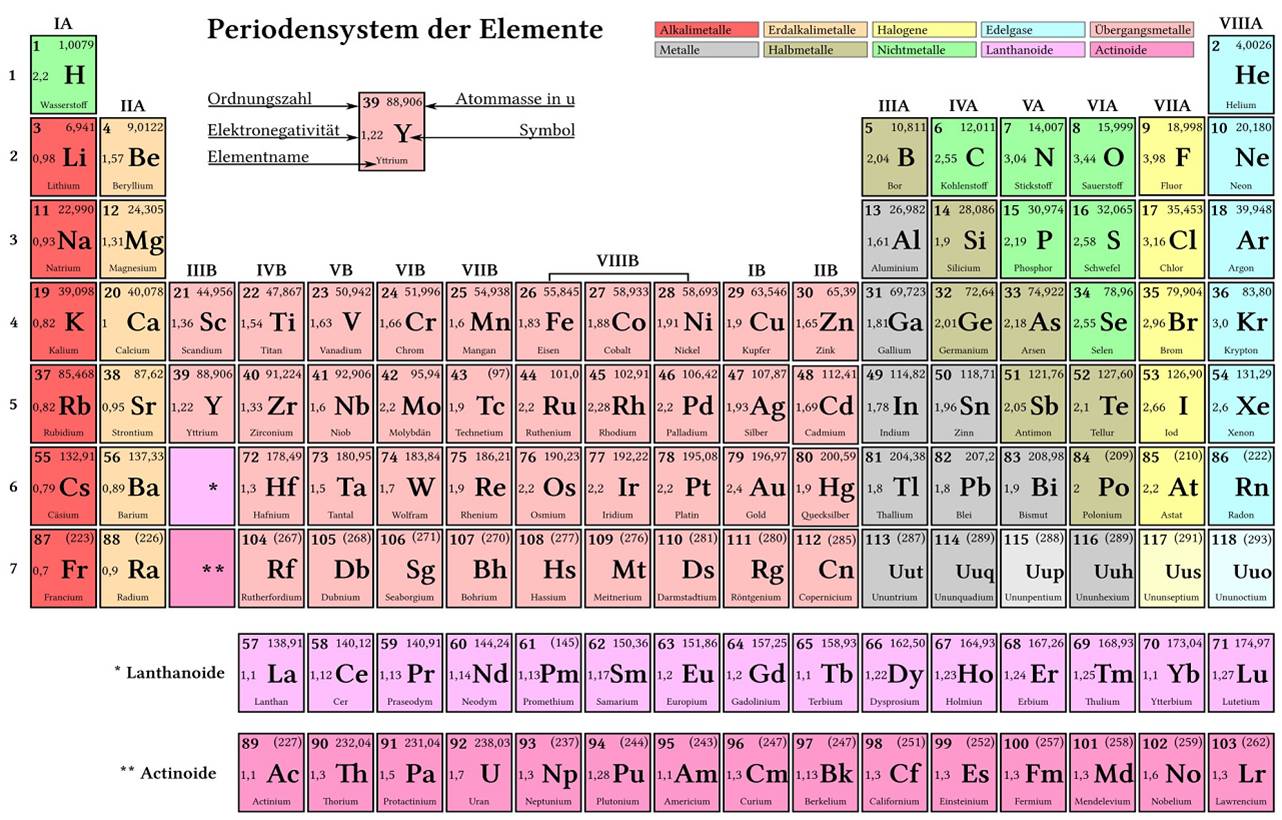
Chemisches Gleichgewicht
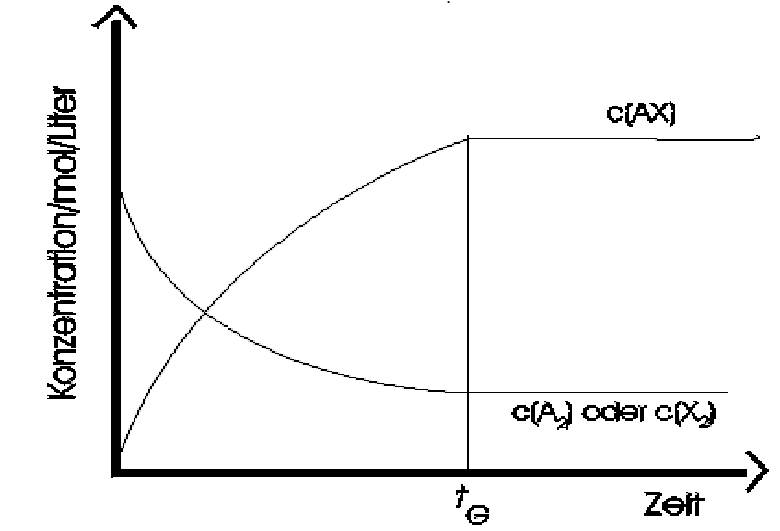
Katalysator
Wirkprinzip (graphisch):
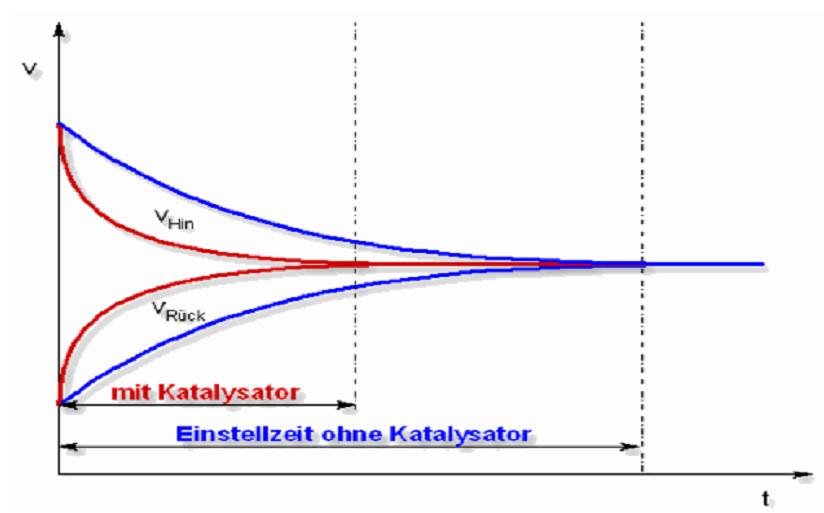
Katalysator
Katalysator bei exothermen Reaktionen:
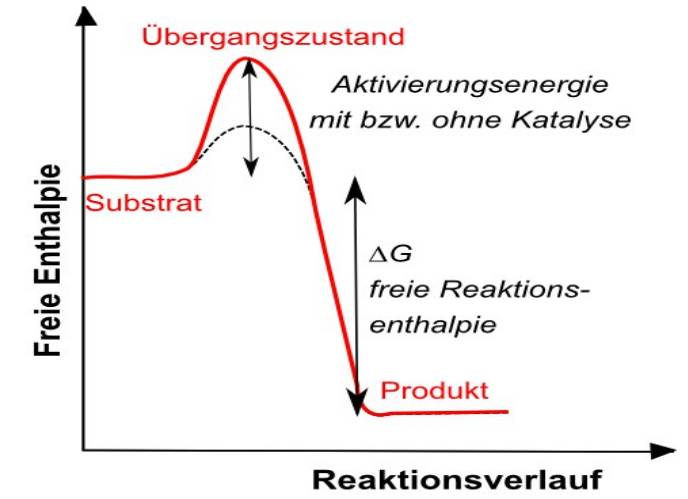
Katalysator
Katalysator bei endothermen Reaktionen:
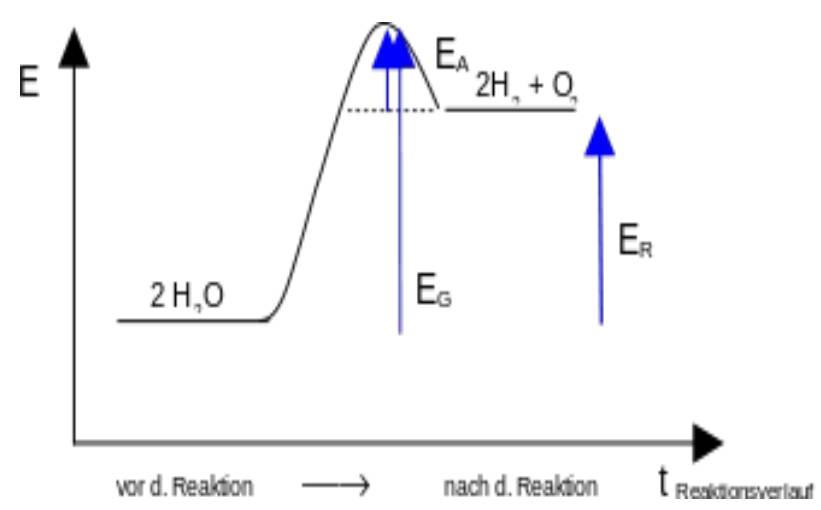
Stöchiometrisches Rechnen
Konstanten/Grundgleichungen:
- Konstanten univ. Gaskonstante R = 8.314 [ J mol-1 K-1]
- Avogadro-Zahl NA = 6.022•1023 [mol-1]
- Faraday-Konstante F = 96485 [ C mol-1]
- Umrechnungen Druck 1 atm = 760 Torr = 1.013 bar = 101300 Pa
- Temperatur T [K] = t [°C] + 273.15
- Stoffmenge n = m/M; n Stoffmenge [mol]; m Masse [g]; M Molare Masse [g mol-1]
- n = N/NA N Teilchenzahl; NA Avogadro-Konstante
Formeln:
c = n/V
- c Stoffmengenkonzentration [mol l-1] (früher: „Molarität“)
- n Stoffmenge gelöster Stoff [mol] V Volumen Lösung
Χ = mi/V(l)
- c∗ Massenkonzentration von i [g l-1]
p V = n R T
- R univ. Gaskonstante [J mol-1 K-1]
|